分享:


摘 要
本文使用带有微透镜阵列(MLA)和衍射光学元件(DOE)的1064nm皮秒激光,来评估激光诱导的光学击穿(LIOB)与皮肤类型的相关性。通过对黑色皮肤组织和白色皮肤组织的检查,来比较评估激光诱导皮肤空泡化的LIOB效应。在能量密度为3.0J/cm2的照射下,黑色皮肤显示,相比于DOE(180-280μm;40μm),MLA产生的激光诱导空泡分布的更深(180-400μm),其大小为67μm。然而,与黑色皮肤的 MLA 相比,白色皮肤的MLA 分布更深(125-700μm),产生的空泡更大(134μm),数量更少。在白色皮肤中,DOE不产生激光诱导的空泡化。皮秒激光治疗后,具有较高散射的白色皮肤组织可能导致更深的空泡化。进一步的研究有望确定各种皮肤类型的好治疗条件。
关键词:衍射光学元件,Fitzpatrick皮肤类型,激光诱导的光学击穿,微透镜阵列,皮秒激光治疗
引言
黄褐斑(发生在妊娠期),是一种常见的色素性疾病,由皮肤表皮层和真皮层的色素过度沉着而形成。这种疾病经常发生于暴露在阳光下的面部突出区域,如脸颊、上唇和前额。黄褐斑发生于所有人群中,并且通常皮肤上会伴随产生深色斑点(棕色、灰色和黑色)。黄褐斑产生的原因有:紫外线(UV)、皮肤中黑色素的沉淀聚集、怀孕、遗传和荷尔蒙失调等。然而,黄褐斑的确切发病机制尚未清楚。黄褐斑主要发生在Fitzpatrick IV-VI型皮肤中,因为Fitzpatrick量表是根据皮肤中黑色素细胞的数量和皮肤对阳光照射的反应情况而制定的皮肤类型分类系统。然而,由于Fitzpatrick I-III型皮肤对紫外线的敏感度较高,因此也很容易发生黄褐斑。
皮秒激光治疗因其非侵入性和恢复时间短的优点,常被用于治疗色素性皮肤疾病。皮秒激光在脉冲宽度(数百皮秒)内,通过皮肤中的多光子电离产生高压(2GPa)和高温(2000-4000K)。此外,高压和高温都会导致等离子体膨胀,并产生冲击波,从而导致皮肤内部出现空泡化,这被称为激光诱导的光学击穿(LIOB)。LIOB引起的激光诱导的空泡化会破坏表皮层和真皮层中的黑色素,但不会造成热损伤或将热损伤降低到最小,同时诱导空泡内的胶原蛋白再生,恢复皮肤状态。为了减少不必要的热损伤,临床上将微透镜阵列(MLA) 和衍射光学元件(DOE)与皮秒激光系统一起使用,MLA具有类似高斯的微束分布,而DOE具有类似平坦的微束分配。由于固有的光学特性,任何透镜都需要根据黄褐斑的情况选择。例如,MLA用于治疗位于真皮层的深色黄褐斑,而DOE用于去除广泛分布在皮肤中的浅色黄褐斑。尽管成功去除了黄褐斑,皮秒激光治疗的临床结果通常取决于皮肤类型。
本研究旨在比较评估在两种不同能量密度(H0,J/cm2)下,用具有MLA和DOE的 1064nm皮秒激光照射后,LIOB效应与两种不同皮肤类型(Fitzpatrick I和VI型皮肤)的相关性。我们假设,在相同条件下,相比于黑色素指数低且散射性高的亮色皮肤,深色皮肤在皮肤真皮深层中产生的空泡更大。使用具有MLA和DOE的1064nm皮秒激光系统测试两种离体猪皮组织(黑色和白色),以比较激光诱导皮肤层中空泡的分布和位置。对其进行组织学分析,定量评估基底膜下激光诱导空泡的深度、大小以及分布情况。
实验
2.1光源
LIOB实验中,1064nm Nd:YAG皮秒激光系统(在半峰全宽[FFWH]处,脉宽=450ps;Picore,韩国釜山Bluecore公司)与MLA(熔融石英,圆形整体光束直径=4mm,微光束直径=220μm,37个微光束,焦距=40mm;韩国釜山Bluecore公司)和DOE(熔融石英,矩形整体光束尺寸=4 mm,微光束直径=165μm,49个微光束,焦距=40 mm;韩国釜山Bluecore公司)一起使用。用MLA和DOE分别对入射的整体光束进行分级处理,大限度地提高激光诱导LIOB后的皮肤空泡化。MLA和DOE采用了两种能量密度(H0=3.0和6.0J/cm2)来比较不同皮肤组织中激光诱导的空泡化程度。为了向靶组织提供相等的能量密度,MLA的微光束能量为10.3和20.5mJ/微束(整体光束能量/脉冲=0.38和0.76J),DOE的微光束能量为9.8和19.6mJ/微束(整体光束能量/脉冲=0.48和0.96J)。根据初步研究,为了在基底膜下产生激光诱导的空泡化,同时对组织表面的损伤降到低,聚焦深度设为35mm(从透镜到靶组织)。MLA和DOE以能量密度为3.0J/cm2的激光照射在黑色调光纸上,通过评估单个微束的功率密度来比较光束的空间分布。
2.2离体实验
从CRONEX Corp(韩国首尔)购买的黑色和白色小型猪皮组织(Cronex Mpig;年龄:6个月;重量:30-65 kg),用于离体实验。本次研究为了保证相同的CIE值,每种皮肤都使用一只猪来进行实验。从每只小型猪的腹部损伤处,随机采集大小为45cm2的新鲜皮肤作为样本(N=5)。然后,在测试之前,将所有制备的样品储存在4℃下,尽量减少脱水,防止物理变形。在实验前,进行了国际照明委员会(CIE)Lab色彩空间测试,通过量化比较黑白皮肤组织的感知亮度(L*)、红/绿值(a*)和蓝/黄值(b*),从而对皮肤颜色进行分类,并与Fitzpatrick皮肤类型匹配一致。使用数码相机拍摄每个组织表面。Image J(国家卫生研究所,贝塞斯达,马里兰州)用于将每个采集的图像转换为二进制图像,然后分成三色Lab堆栈图像,以测量Lab颜色值。将测量值与von luschan量表(分为36个阶段)进行对比,以确认测试皮肤类型与Fitzpatrick皮肤类型的相关性(I=0-6,II=7-13,III=14-20,IV=21-27,V=28-34,VI=35-36)。本研究评估了在1064nm皮秒激光照射期间,LIOB效应与皮肤类型的相关性。因此,通过测试两种不同的皮肤颜色(黑色和白色),来代表Fitzpatrick VI和I的皮肤类型。每个组织样本最初处于一个平移阶段,在单脉冲照射后横向移动50μm。所以,每次激光治疗时,需对皮肤进行20次激光照射(总治疗长度=1mm)。拍摄表面图像以比较每种皮肤类型表面上的微束斑的空间分布。
2.3组织学分析
将激光照射后的组织在10%中性福尔马林溶液(Sigma Aldrich,圣路易斯,密苏里州)中固定2天。之后,切成厚度为5μm的蜡块以制备6个滑块(N=6),并用苏木精和伊红(H&E)染色进行组织学分析。使用光学显微镜(Leica DM500,Leica,Wetzlar,Germany)对所有组织切片进行×100倍和×400倍成像。病理学家鉴定了激光诱导的空泡,并对其形状、大小和位置进行了表征。空泡不同于皮肤组织中具有孔状结构的汗腺和毛囊。Image J用于测量组织内激光诱导空泡的尺寸(深度和面积),还可估计空泡的覆盖率,以比较不同皮肤深度下,黑色和白色皮肤组织中的空泡分布。为了进行定量分析,将组织学图像转换为二进制图像,阈值设置为约20%,并对激光诱导的空泡进行分类。转换后,将所有图像分割为40μm高度,根据皮肤深度量化空泡面积。然后,通过将激光诱导空泡的面积除以组织总面积来计算分割图像。使用SPSS软件22(SPSS Inc.,Chicago,Illinois)对非参数统计分析进行Mann-Whitney U检验。P<0.05被认为具有统计学意义。
结果
图1显示了离体猪皮组织对MLA和DOE激光照射的激光诱导反应。图1A显示了通过von luschan量表确定的Fitzpatrick皮肤类型的CIE Lab色彩空间分布。Fitzpatrick皮肤类型的CIE Lab颜色值分布广泛(L*=13-96,a*=-3-18,b*=-6-39)。黑色皮肤的CIE Lab颜色值为L*=29,a*=4.4,b*=7.4,对应于Fitzpatrick V和VI型皮肤(L*=13-28,a*=5.7-18,b*=-6-20)。另一方面,白色皮肤的L*=70,a*=2.5,b*=7.8,代表Fitzpatrick I和II型皮肤(L*=96.4~96.5,a*=-0.4-0.03,b*=4.8-5.9)。可以看出,白色皮肤的L*、a*和b*值低于Fitzpatrick皮肤类型,这可能是因为组织提取后没有血流的原因。图1B显示了用MLA和DOE以3.0J/cm2(顶部)和6.0J/cm2(底部)照射20次后,黑白皮肤表面的俯视图。MLA产生圆形的轮廓光束,而DOE产生矩形轮廓光束。图1C显示了黑色调光纸上MLA和DOE的光束分布(H0=3.0J/cm2)。MLA的光斑尺寸偏差相对较大,中心处的光强度较高。另一方面,DOE产生了相对均匀的光束分布。由于深色皮肤对光的强烈吸收,无论哪种透镜,黑色皮肤都能清楚地显示出重叠的整体束斑。另一方面,白色皮肤在MLA和DOE照射后,显示出模糊或不太明显的整体束斑和热损伤痕迹。

图1. 在H0=3.0和6.0J/cm2下用微透镜阵列(MLA)和衍射光学元件(DOE)照射后,不同肤色(黑色和白色)离体猪皮组织的比较:(A)Fitzpatrick I–VI型皮肤和受试皮肤组织(圆形)的CIE Lab颜色空间值(A*=红色/绿色;b*=蓝色/黄色;L*=感知亮度)分布,(B)激光照射皮肤的俯视图,以及(C)在3.0J/cm2(bar=1mm)下MLA和DOE的微束图像和光束分布。值得注意是,在照射期间,整体光束从左(橙色虚线)移动到右(红色虚线)(横向移动=50μm/脉冲;共20次照射;bar=2mm;green bar=1mm)
图2显示了在H0=3.0 J/cm2下,用MLA和DOE进行激光照射后,黑白皮肤组织的HE染色图像。黑色皮肤中,MLA和DOE明显能在基底膜下产生激光诱导的空泡。根据图2A,MLA在黑色皮肤中的真皮乳头层到真皮网状层深度中,产生了多个小空泡。相比于黑色皮肤,在白色皮肤中,观察到了更大和更深的空泡(黑色皮肤的空泡深度=283±114μm,白色皮肤的空泡深度为368±171μm;P<.01,黑色皮肤的空泡大小=67±34μm,而白色皮肤的空泡大小为134±100μm;P<.001;图2A)。另一方面,与MLA相比,DOE在黑色皮肤真皮乳头层附近,激光诱导产生的空泡数量相对较少(空泡深度=140±62μm;图2B)。然而,白色皮肤在真皮乳头层中,没有表现出空泡化的光破坏性损伤。
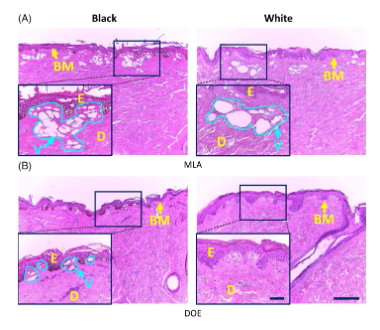
图2. (A)微透镜阵列(MLA)和(B)衍射光学元件(DOE)在H0=3.0J/cm2(100和bar=200μm)照射后,黑色(左列)和白色(右列)猪皮组织的组织学图像(HE染色)。注意,入口(400和bar=50μm)表示皮肤表面的放大区域(黑色实线;E:表皮,D:真皮,BM:基膜,V:激光诱导的空泡)
图3显示了在H0=6.0 J/cm2下,用MLA和DOE进行激光照射后,黑白皮肤组织的HE染色图像。对于黑白皮肤组织,MLA和DOE在基膜下产生空泡。在图3A中,MLA在黑色和白色皮肤组织中产生了空泡的深度分布。然而,白色皮肤在上表皮进行了光击穿消融,产生了比黑色皮肤更大的空泡(即,黑色空泡大小为70±37μm,白色空泡大小为162±98μm;P<0.001)。在图3B中,DOE在黑色皮肤的真皮乳头层附近,产生了激光诱导的空泡(空泡深度=210±54μm),但尺寸小于MLA(P<0.001)。然而,DOE照射后,在白色皮肤中未发现激光诱导的空泡化。
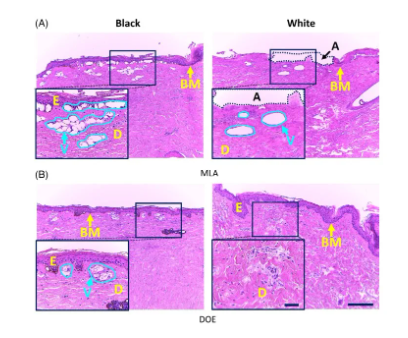
图3. (A)微透镜阵列(MLA)和(B)衍射光学元件(DOE)在H0=6.0J/cm2(100和bar=200μm)照射后,黑色(左列)和白色(右列)猪皮组织的组织学图像(HE染色)。值得注意的是,入口(400和bar=50μm)表示皮肤表面的放大区域(黑色实线;E:表皮,D:真皮,BM:基膜,V:激光诱导的空泡)
图4比较了不同空泡深度和H0下,黑白皮肤组织中激光诱导的空泡数量。图4A显示,无论哪种皮肤类型,与DOE(160至280μm)相比, MLA产生的空泡更多,并且空泡化的范围更深(160至550μm)。对于黑色皮肤,3.0J/cm2的MLA和DOE在~200μm的深度产生的空泡数量最多。另一方面,MLA激光照射后,相比于黑色皮肤,白色皮肤产生的空泡化更深(黑色皮肤为~200μm,白色皮肤为~380μm),但空泡数量相对较少(黑色皮肤为~110个,白色皮肤为~60个;P<0.05;图4A)。然而,在用DOE照射白色皮肤后,没有观察到或观察到极小的空泡。当H0=6.0J/cm2时,MLA和DOE在黑色皮肤上产生的空泡数量,在深度为200μm时最多(图4B)。较高的H0会导致平均空泡深度发生显著变化(黑色皮肤中,3.0J/cm2的空泡深度=283±114μm,6.0J/cm2的空泡深度为294±126μm;P=.50)。另一方面,在用MLA和DOE照射后,白色皮肤产生的空泡数量较少。
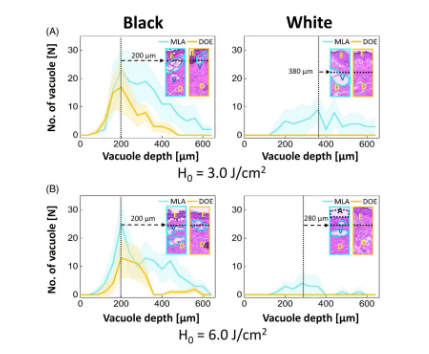
图4. 用显微透镜阵列(MLA)和衍射光学元件(DOE)照射后,定量分析从组织学图像测量的黑白皮肤组织:(A)H0=3.0J/cm2和(B)H0=6.0J/cm2处产生的空泡深度与数量的比较。值得注意的是,入口(100)表示组织中的空泡分布(E:表皮,D:真皮,V:激光诱导的空泡,A:消融区域;线周围的填充区域:SD)
图5量化了在H0=3.0和6.0J/cm2下,用MLA和DOE照射后,黑色和白色皮肤组织中空泡尺寸大小的函数。根据图5A,H0=3.0J/cm2下的MLA和DOE在黑色皮肤中产生的空泡数量最多,大小为70μm。MLA产生的空泡数量比DOE多(MLA为~170个,DOE为~70个;P<0.05)。另一方面,相比于黑色皮肤,在MLA照射后,白色皮肤的基底膜下发现了数量较少但尺寸较大的空泡(平均大小=134±100μm)(图5A)。DOE在真皮乳头层中引发了光损伤,且没有激光诱导的空泡产生。图5B表明,尽管H0较高,但在黑色皮肤中,MLA和DOE产生的激光诱导空泡数量较少,大小为55-70μm。MLA产生的空泡多于DOE(P<0.05)。另一方面,在白色皮肤中,MLA产生了数量较少的大空泡(空泡大小=162±98μm)。DOE在白色皮肤中没有产生激光诱导的空泡化,并伴有真皮层的光损伤。
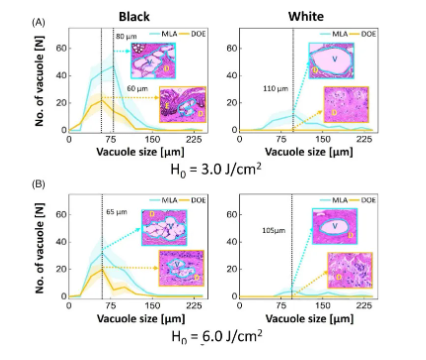
图5. 用显微透镜阵列(MLA)和衍射光学元件(DOE)照射后,定量分析从组织学图像测量的黑白皮肤组织:(A)H0=3.0J/cm2和(B)H0=6.0J/cm2处产生的空泡大小与数量的比较。值得注意的是,入口(400)表示平均空泡大小(E:表皮,D:真皮,V:激光诱导的空泡泡;线周围的填充面积:SD)
图6显示了在H0=3.0和6.0J/cm2条件下,MLA和DOE照射黑白皮肤组织后,激光诱导的空泡覆盖率随皮肤组织深度的变化。空泡覆盖率代表了皮肤目标区域内产生空泡的相对空间分布。在图6A中,无论任何皮肤类型,在H0=3.0J/cm2时,MLA和DOE在基膜下都产生了大量的空泡。在黑色皮肤中,MLA产生的空泡覆盖范围更深(180-400μm),而DOE的覆盖范围相对较窄(180-280μm)。MLA和DOE分别在360μm和260μm处,产生了大覆盖率,分别为22%和17%。MLA的平均覆盖率为14%,DOE的平均覆盖率为6%。相对于黑色皮肤,在白色皮肤中,MLA在更深的分布(125-700μm)中产生了少量的空泡。大空泡覆盖率为22%,出现在460μm处(平均覆盖率为15%)。另一方面,DOE在白色皮肤中没有产生激光诱导的空泡化(覆盖率为0%)。图6B显示了在H0=6.0J/cm2下,用MLA和DOE照射后的空泡覆盖率。在黑色皮肤中,MLA的空泡分布比DOE更深(即,MLA为180-550μm,DOE为225-400μm)。MLA在360μm处,产生了空泡覆盖率大,为24%,而DOE在300μm处,产生了大覆盖率,为14%。MLA和DOE的平均覆盖率分别为13.5%和5.3%,高于H0=3.0J/cm2时的覆盖率。对于白色皮肤,MLA在表皮层和真皮乳头层中显示出光消融,导致相比于在H0=3.0J/cm2的照射下,白色皮肤的空泡在更窄的分布中(125-750μm)数量更少(图3A)。大空泡覆盖率为21%,出现在375μm处(平均覆盖率=10%)。但DOE在白色皮肤中仍然没有引起激光诱导的空泡化(0%覆盖率)。表1总结了激光诱导的空泡化与皮肤颜色、能量密度和透镜类型的相关性。
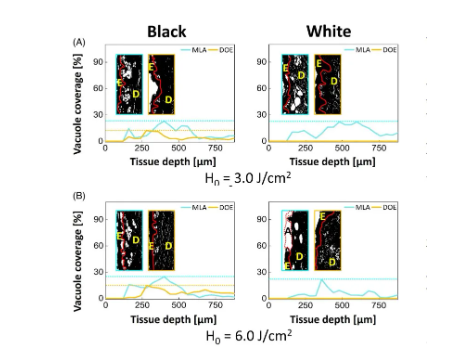
图6. (A)H0=3.0J/cm2和(B)H0=6.0J/cm2的条件下,用微透镜阵列(MLA)和衍射光学元件(DOE)照射黑白皮肤组织后,定量比较空泡覆盖率随深度的变化。值得注意的是,入口(100)表示对组织中空泡进行二进制图像分类(E:表皮,D:真皮,红线:基底膜,A:烧蚀区域)
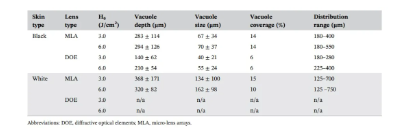
表1. 激光诱导的空泡化与皮肤类型、透镜类型和H0的相关性
讨论
由于黄褐斑在所有人群中发病率都很高,因此,治疗黄褐斑已被广泛研究。尽管目前的临床治疗主要集中于黄褐斑的位置、大小和深度,但治疗条件需要根据含有不同类型黑色素的皮肤进行优化。当前研究的目的是通过使用带有MLA和DOE的1064nm皮秒激光,评估LIOB效应与两种不同皮肤类型(黑色和白色)的相关性。CIE Lab色彩空间将测试的黑色和白色皮肤组织分类为Fitzpatrick VI和I型皮肤。由于组织提取后,离体猪皮组织在血流、温度和水含量方面不同于人类皮肤特性。但,离体皮肤能够显示出适合Fitzpatrick皮肤类型的值。黑色皮肤在基底膜附近出现了激光诱导的空泡化(MLA的深度=283μm,DOE的深度=140μm),且形成了的空泡大小相对均匀(例如,在3.0J/cm2下,MLA为67μm,而DOE为40μm)。另一方面,用MLA照射的白色皮肤,在较深的位置产生了较大的空泡,但数量较少,这可能是由于高散射特征造成的(3.0J/cm2下,MLA的深度=368μm,尺寸=134μm;图4-6)。值得注意的是,微束能量较小的DOE没有产生激光诱导的空泡化。图6显示,不同皮肤类型之间,平均空泡覆盖率无明显变化,但空泡数量、大小和分布变化却很明显(图4和图5)。两种皮肤类型之间的覆盖率相当,这意味着白色皮肤比黑色皮肤产生的空泡更大,但数量较少。可以想象,黑色素含量较高的黑色皮肤可以立即吸收光,在组织中产生LIOB,从而在皮肤中形成空泡。相比之下,白色皮肤由于具有高镜面反射和散射,对光吸收相对较少,最终导致组织中的LIOB较弱。若采用较高的能量密度来增加LIOB效应,那么表皮层和真皮乳头层就会发生了光损伤(图3)。
最近,许多研究证明了皮秒激光治疗后LIOB对不同皮肤类型的影响。Moustafa等人用1064和532nm皮秒激光(H0=4J/cm2)检查了Fitzpatrick III和IV型皮肤。他们的结果表明,在第一次治疗后,第11至16周的随访中,III型皮肤患者的色素沉着清除率为100%,IV型皮肤患者为75%。与黑色皮肤相比,白色皮肤中产生的较大空泡(图2、图3和图5)可以更有效地去除色素以及胶原蛋白再生。Nguyen等人通过使用H0=1.05至1.12J/cm2的1064nm激光,去除了Fitzpatrick III到IV型皮肤中的色素沉着病变。III至IV型皮肤的色素沉着清除率分别为75%至90%,而皮肤中的黑色素指数在产生光致破裂中起着重要作用。白色皮肤中较低的黑色素指数和高散射特征可能导致入射光子空间分布的更广,从而扩大激光诱导的空泡化。大空泡可以有效地去除皮肤中的色素。然而,由于胶原重塑,大空泡可能比小空泡的愈合时间更长。因此,可以向白色皮肤施加少量的激光脉冲,使其具有等效LIOB效应的同时减小空泡的大小。
本研究通过测试两种不同颜色的离体猪皮来比较LIOB效果。尽管白色皮肤在实验上显示出比黑色皮肤的激光诱导的空泡化更大更深,但由于没有血流、水分和恒定的皮肤温度,与人类皮肤组织具有不同的光学性质(吸收和散射)。所以,在1064nm皮秒激光治疗期间,人类皮肤组织的不均匀光学特性可以改变LIOB效应的程度。此外,本研究通过量化皮肤颜色的CIE Lab颜色值和激光诱导空泡的程度,比较了两种不同皮肤类型对皮秒激光治疗的反应。与MLA相比,无论何种能量密度,DOE在白色皮肤中都没有出现空泡化,这可能是由于微束能量级别较低。因此,应优化各种照射条件,例如整体光束大小、聚焦深度和能量密度,从而在组织中实现激光诱导空泡的较大化。对于临床转化,需进行进一步研究,以评估LIOB在恢复时间和黄褐斑清除方面与人类皮肤类型的相关性。
结论
本次研究通过使用MLA和DOE辅助的1064nm皮秒激光,证明了LIOB对不同离体猪皮类型的空间相关性。与黑色皮肤相比,白色皮肤的高散射和表面较少的光吸收,可能会导致在较深位置下,激光诱导空泡数量减少。进一步的研究,将验证本次对不同人类皮肤类型的研究结果,从而保证临床应用的有效性和安全性。
芙迈蕾
苏州芙迈蕾医疗科技有限公司核心创始团队来自北京大学等海内外知名高校。芙迈蕾以合规为基础,以产品力为核心,专注于先进医美光电设备的设计、研发及应用落地,致力于成为全球先进医美光电设备领域的龙头企业、诊疗一体化智能解决方案的提供者,以及医美数据整合平台的开拓者。
通过攻坚一系列底层的关键技术,芙迈蕾现已自主研发出皮秒激光治疗仪、长脉冲激光治疗仪、强脉冲光治疗仪、光声成像皮肤检测设备和冷空气治疗仪等多款先进医疗设备,并持续深耕产品核心技术的研发,用更高效的技术解决方案,造福广大的求美者。
坚持科技向善,芙迈蕾将携手产业和生态合作伙伴,为全球医美市场带来更多安全有效的医美光电设备与诊疗一体化解决方案。